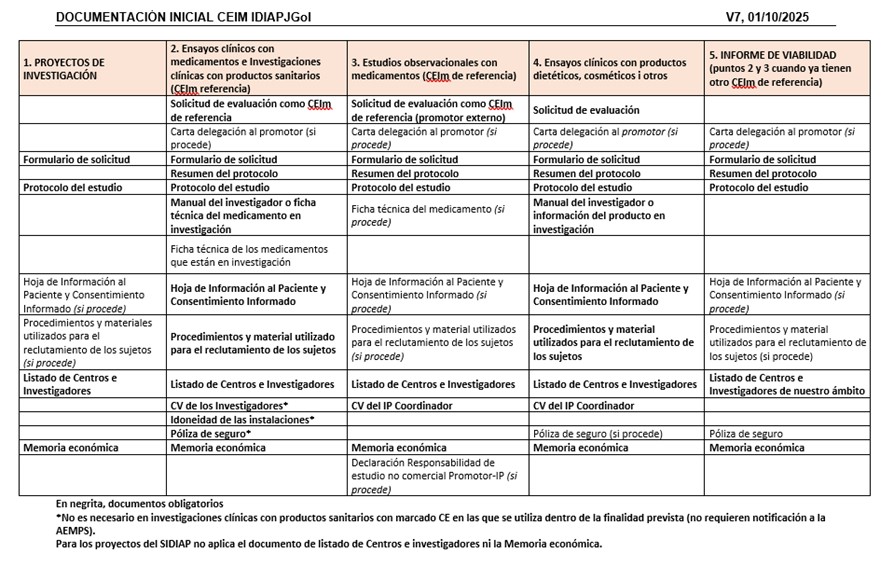
Es necesario realizar una carta de Solicitud al CEIm IDIAP Jordi Gol cuando tenga que ser el CEIm de referencia para un estudio observacional con medicamentos (EOm) o una investigación clínica con productos sanitarios.
Si se trata de un proyecto sin interés comercial es necesario aportar la declaración de responsabilidad de estudio no comercial por parte del promotor-IP (en su caso)
Si se quiere realizar un EOm prospectivo es necesario solicitar la valoración por parte del Departamento de Salud antes de firmar el contrato, a excepción de los estudios que tengan como promotor una administración publica y aquellos en los que se acredite que se trata de una investigación clínica sin ánimo comercial. Puede encontrar más información en el siguiente enlace:
https://medicaments.gencat.cat/ca/professionals/recerca/estudis-observacionals-amb-medicaments/